Spośród wszystkich technik chromatograficznych, chromatografia powinowactwa (Affinity chromatography) jest najbardziej specyficzna. Wszystkie omawiane dotychczas techniki: chromatografia jonowymienna, wykluczenia mas czy RP-LC, opierały się o właściwości fizykochemiczne cząsteczek. W tym przypadku interakcja pomiędzy analitem a fazą stacjonarną opiera się o konkretną unikalną biochemiczną cechę. To właśnie sprawia, że chromatografia powinowactwa jest w stanie oczyścić konretne białko spośród tysięcy innych i jest powszechnie stosowana w preparatyce. W przypadku niektórych białek mówimy o czystości przekraczającej nawet 95% w pojedynczym etapie oczyszczania.

Czym jest chromatografia powinowactwa?
Chromatografia powinowactwa to technika rozdzielcza oparta na wysoce swoistym, odwracalnym oddziaływaniu biologicznym między analizowaną cząsteczką (analitem) a specyficznym ligandem związanym kowalencyjnie z nierozpuszczalną matrycą.
Historyczne korzenie tej metody sięgają początku XX wieku, jednak jej gwałtowny rozwój nastąpił w 1968 roku, kiedy to Cuatrecasas, Wilchek i Anfinsen opisali zastosowanie aktywowanej agarozy do unieruchamiania ligandów. Istota metody tkwi w termodynamicznej i stereochemicznej komplementarności dwóch cząsteczek. Mechanizm ten przypomina model „klucza i zamka”, gdzie tylko specyficzna struktura może dopasować się do miejsca wiążącego liganda.
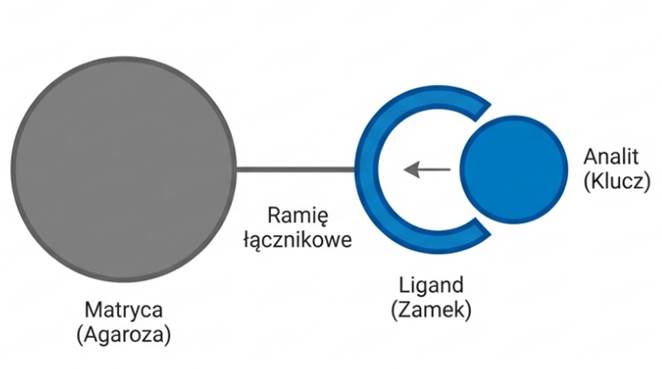
W skrócie. W chromatografii powinowactwa z kolumną zwiążą się jedynie te cząsteczki, które wchodzą w specyficzne biochemiczne interakcje z ligandem unieruchomionym na kolumnie. Pozostałe cząsteczki przepłyną przez kolumnę niezwiązane.
Mechanizm chromatografii powinowactwa
Skuteczność chromatografii powinowactwa opiera się na sumarycznym efekcie słabych oddziaływań niekowalencyjnych, które w odpowiedniej konfiguracji przestrzennej tworzą trwałe połączenie. Do najważniejszych należą:
- Wiązania wodorowe: Kluczowe dla orientacji cząsteczki w miejscu wiążącym.
- Oddziaływania elektrostatyczne: Solne mostki między grupami funkcyjnymi o przeciwnych ładunkach.
- Siły van der Waalsa i oddziaływania hydrofobowe: Odgrywają decydującą rolę w stabilizacji kompleksu, szczególnie w środowisku wodnym.
Typy oddziaływań biospecyficznych
W zależności od natury partnerów interakcji, wyróżniamy kilka podstawowych mechanizmów:
- Antygen – Przeciwciało: Najbardziej specyficzny model, wykorzystywany w immunopuryfikacji. Na złożu kolumny unieruchomione są przeciwciała specyficzne dla konkretnego antygenu, który chcemy oczyścić.

- Enzym – Substrat / Inhibitor: Wykorzystuje powinowactwo centrum aktywnego enzymu do analogów substratu lub inhibitorów.
- Receptor – Ligand: Naśladowanie naturalnych szlaków sygnalizacyjnych, np. wiązanie hormonów przez ich receptory błonowe.

- Kwas nukleinowy – Białko wiążące: Wykorzystywane do izolacji czynników transkrypcyjnych lub polimeraz.

Chromatografia powinowactwa: przykłady
Praktyczne zastosowanie chromatografii powinowactwa ewoluowało od prostych eksperymentów laboratoryjnych do wielkoskalowych procesów przemysłowych. Poniżej przedstawiamy kluczowe systemy wykorzystywane w R&D i produkcji leków.
A. Konkanawalina A (ConA): oczyszczanie glikoprotein
Lektyny to białka posiadające zdolność specyficznego wiązania cukrów. Konkanawalina A (ConA), izolowana z Canavalia ensiformis, jest najczęściej stosowaną lektyną w chromatografii.
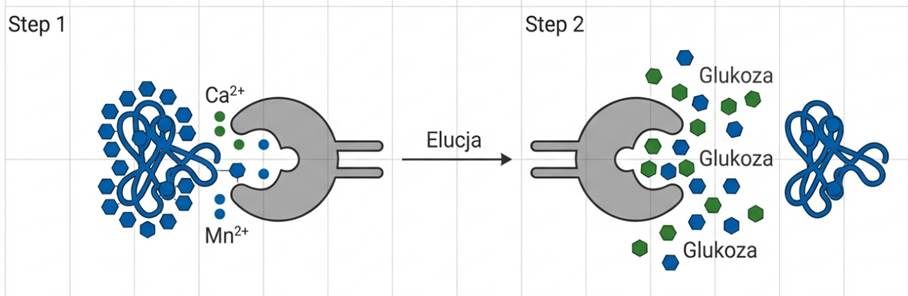
- Mechanizm: ConA wykazuje silne powinowactwo do terminalnych reszt α-D-mannopiranozy i α-D-glukopiranozy. Po nałożeniu próbki na kolumnę, glikoproteiny specyficznie łączą się z ConA poprzez te reszty cukrowcowe. Pozostałe białka zostają wypłukane z kolumny. Elucja zachodzi poprzez zwiększenie udziału glukozy w fazie ruchomej, która konkuruje o miejsce wiązania z ConA.
- Wymagania kofaktorowe: Aktywność wiążąca ConA jest ściśle zależna od obecności jonów metali dwuwartościowych Ca2+ i Mn2+.
- Zastosowanie: Separacja glikoprotein osocza, oczyszczanie enzymów lizosomalnych oraz analiza profilu glikozylacji w badaniach nowotworowych.
B. Białko A (Protein A): Oczyszczanie przeciwciał
W dobie rozkwitu immunoterapii, białko A (pochodzące ze złocistego gronkowca Staphylococcus aureus) stało się standardem w oczyszczaniu przeciwciał klasy IgG.
- Mechanizm: Białko A wiąże się specyficznie z fragmentem Fc przeciwciał.
- Specyfika elucji: Wiązanie zachodzi przy pH fizjologicznym (ok. 7.2), natomiast elucja wymaga obniżenia pH do wartości 3.0–3.5. Powoduje to protonację reszt histydynowych w miejscu kontaktu, co generuje odpychanie elektrostatyczne i dysocjację kompleksu.
- Znaczenie przemysłowe: Jest to kluczowy etap typu capture (wychwytu) w produkcji leków opartych o przeciwciała monoklonalne.
C. IMAC: Immobilized Metal Affinity Chromatography
Jedna z najpopularniejszych metod w biologii molekularnej, wykorzystująca powinowactwo aminokwasów (głównie histydyny) do jonów metali przejściowych (Ni2+, Co2+, Cu2+, Zn2+).
- Tagi histydynowe: W niektórych białkach rekombinowanych wprowadza się sekwencje 6x His na N- lub C-końcu białka. Pozwala to na jego łatwe wyłapanie na złożu chelatującym jony niklu.
- Elucja: Najczęściej stosuje się gradient stężenia imidazolu, który jako analog bocznego łańcucha histydyny współzawodniczy o miejsce wiążące przy jonie metalu.
Zastosowania chromatografii powinowactwa
Chromatografia powinowactwa ma szereg zastosowań
Zastosowania Analityczne
W skali mikro, chromatografia powinowactwa służy do precyzyjnej diagnostyki i badań podstawowych:
- Diagnostyka medyczna: Oznaczanie poziomu hemoglobiny glikowanej (HbA1c) przy użyciu powinowactwa boronianowego.
- Proteomika: Wzbogacanie próbek o rzadkie białka sygnałowe lub usuwanie białek o wysokiej liczebności (np. albuminy z surowicy), co pozwala na detekcję markerów nowotworowych obecnych w stężeniach pikogramowych.
- Badania interakcji: Wyznaczanie parametrów kinetycznych układów receptor-ligand
Zastosowania Preparatywne
Dzięki specyficznemu wiązaniu konkretnych białek, chromatografia powinowactwa doskonale się sprawdza w preparatyce laboratoryjnej i przemysłowej
- Produkcja leków biologicznych: Oczyszczanie białek rekombinowanych i hormonów (np. przeciwciał monoklonalnych)
- Bezpieczeństwo wirusowe: Wykorzystanie specyficznych ligandów do usuwania zanieczyszczeń wirusowych z preparatów krwiopochodnych.
- Wielka skala: Kolumny o średnicy przekraczającej 1 metr, zdolne do przetwarzania tysięcy litrów hodowli komórkowej.
Podsumowanie
Największą zaletą chromatografii powinowactwa jest niewątpliwie selektywność, która nie ma sobie równych wśród innych metod separacji. Wyzwania, przed którymi stoi ta dziedzina, to przede wszystkim wysoki koszt matryc biologicznych oraz ich ograniczona stabilność chemiczna (np. wrażliwość białka A na drastyczne procedury mycia kolumn).
Przyszłość należy do ligandów syntetycznych oraz aptamerów (cząsteczek DNA/RNA), które oferują trwałość polimerów syntetycznych przy zachowaniu biologicznej precyzji rozpoznawania. Integracja chromatografii powinowactwa z systemami ciągłymi (np. Periodic Counter-current Chromatography) już teraz rewolucjonizuje wydajność produkcji bioterapeutyków.
Bibliografia
- Cuatrecasas P., Wilchek M., Anfinsen C.B. (1968). Selective enzyme purification by affinity chromatography. Proceedings of the National Academy of Sciences (PNAS).
- Low D., O’Leary R., Axelsson N.S. (2007). Future of antibody purification. Journal of Chromatography B.
- Urh M., Simpson D., Zhao K. (2009). Affinity Chromatography: General Methods. Methods in Enzymology.
- Hage D.S. (1999). Affinity chromatography: a review of clinical applications. Clinical Chemistry
FAQ – Często Zadawane Pytania
1. Czym różni się elucja specyficzna od niespecyficznej w chromatografii powinowactwa?
Elucja specyficzna polega na dodaniu do buforu wolnego liganda lub jego analogu, który „wypiera” białko ze złoża (np. imidazol w IMAC). Elucja niespecyficzna polega na zmianie warunków fizykochemicznych (pH, siła jonowa), co prowadzi do osłabienia oddziaływań między białkiem a ligandem na złożu.
2. Co to jest „spacer arm” (ramię łącznikowe) i dlaczego jest krytyczne?
Ramię łącznikowe to krótka cząsteczka (np. łańcuch węglowodorowy) wstawiona między matrycę a ligand. Jest niezbędne, aby zredukować zawadę przestrzenną – pozwala ligandowi na swobodne wysunięcie się w głąb roztworu, co umożliwia dostęp do głęboko położonych miejsc wiążących w dużych makrocząsteczkach białkowych.
3. Czy chromatografia powinowactwa może być stosowana do usuwania zanieczyszczeń, a nie tylko izolacji produktu?
Tak, jest to tzw. „negatywna chromatografia powinowactwa”. W tym podejściu to zanieczyszczenia (np. albuminy lub pirogeny) wiążą się ze złożem, a pożądane białko przepływa przez kolumnę bez zatrzymania. Metoda ta jest często stosowana w końcowych etapach oczyszczania preparatów farmaceutycznych.
