Zjawiska elektryczne mają wiele zastosowań w analityce laboratoryjnej. Są wykorzystywane choćby w elektroforezie czy spektrometrii mas. Do tej pory opisywaliśmy chromatografię jako rozdział oparty o wielkość cząstek lub ich polarność. Chromatografia jonowymienna (IEC – Ion Exchange Chromatography) wykorzystuje do rozdziału ładunek cząsteczek i ich oddziaływania elektryczne z naładowaną fazą stacjonarną.
Czym właściwie jest chromatografia jonowymienna?
Chromatografia jonowymienna nazywana jest również chromatografią jonową. To technika analityczna i preparatywna, która rozdziela cząsteczki na podstawie ich ładunku elektrycznego netto.
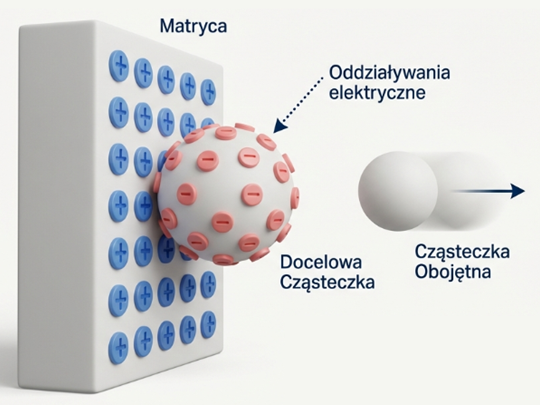
Zasada jest prosta: Chromatografia jonowymienna wykorzystuje fakt, że cząsteczki (np. jony, białka, kwasy nukleinowe) posiadają na swojej powierzchni ładunek dodatni lub ujemny. Jeśli przepuścimy taką mieszaninę przez kolumnę wypełnioną złożem (matrycą) o przeciwnym ładunku, nasze docelowe cząsteczki „przykleją się” do niego, podczas gdy reszta po prostu wypłynie z kolumny.
To, jak trwale cząsteczki będą się trzymać fazy stacjonarnej można ściśle regulować składem fazy ruchomej. W IEC można to zrobić tak precyzyjnie, żeby oddzielić od siebie dwa białka różniące się zaledwie kilkoma atomami, o ile tylko te różnice wpływają na ich wypadkowy ładunek.
Jak działa chromatografia jonowymienna?
Złoże wewnątrz kolumny (faza stacjonarna) posiada na stałe przytwierdzone grupy funkcyjne, które niosą określony ładunek. W trakcie rozdziału na kolumnie jonowymiennej zachodzi kilka zjawisk.
Adsorpcja (Wiązanie): Po wprowadzeniu próbki do kolumny, jony o ładunku przeciwnym do ładunku złoża zaczynają z nim oddziaływać. Powstają wiązania elektrostatyczne. To silne, ale odwracalne przyciąganie. Cząsteczki obojętne lub o tym samym ładunku co złoże mkną przez kolumnę bez zatrzymania.
Równowaga dynamiczna: W kolumnie panuje nieustanna konkurencja. Jony z próbki rywalizują o miejsca wiążące z jonami, które już tam były (tzw. jonami przeciwstawnymi).
Elucja (Uwalnianie): Aby odzyskać „uwięzione” cząsteczki, trzeba zmienić zasady gry. Zazwyczaj robimy to na dwa sposoby:
- Zwiększamy stężenie soli: Dodajemy do układu mnóstwo małych jonów (np. chlorku sodu), które dosłownie „wypychają” nasze białka z miejsc wiążących.
- Zmieniamy pH: Modyfikujemy kwasowość otoczenia, co zmienia ładunek samych cząsteczek. Jeśli białko straci swój ładunek, straci też powód, by trzymać się złoża.
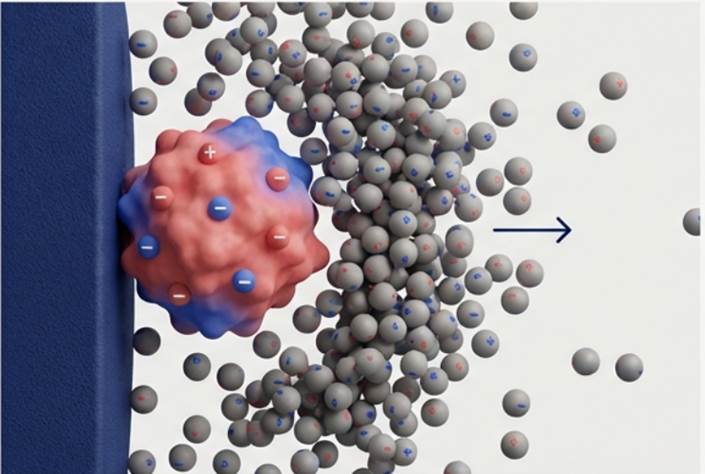
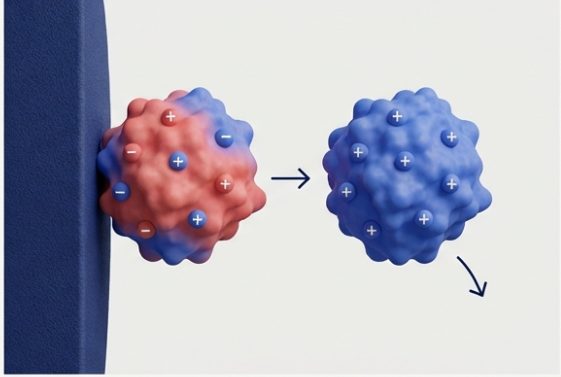
Odpowiednio sterując gradientem jonów lub pH w fazie ruchomej można precyzyjnie wyłapać konkretne białko z mieszaniny.
Podział chromatografii jonowymiennej
Wybór odpowiedniego „magnesu” to klucz do sukcesu. W chromatografii jonowymiennej dzielimy jonowymieniacze na dwie główne kategorie:
1. Kationity (Wymieniacze kationowe)
Posiadają one ładunek ujemny na swojej powierzchni. Jak sama nazwa wskazuje, przyciągają i wymieniają kationy (jony dodatnie). Chromatografia z ich wykorzystaniem to tzw. Chromatografia kationowymienna (CEX – Cation Exchange Chromatography). Tą w zależności od siły kationitów można podzielić na dwie kategorie:
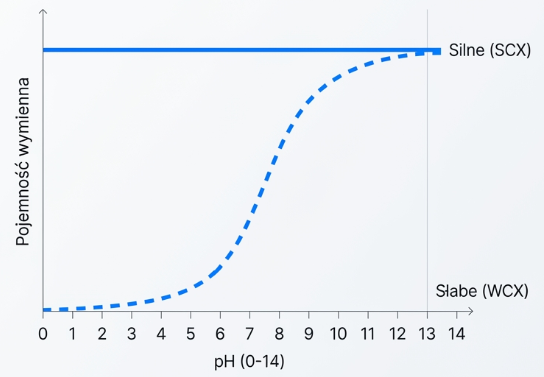
- Silne kationity (SCX – Strong Cation Exchange): Zachowują swój ładunek w bardzo szerokim zakresie pH (np. grupy sulfonowe). Pracują stabilnie niemal w każdych warunkach.
- Słabe kationity (WCX – Weak Cation Exchange): Ich ładunek zależy od pH otoczenia (np. grupy karboksylowe). Dają analitykowi dodatkowe narzędzie kontroli – zmieniając pH, możemy „włączyć” lub „wyłączyć” ich właściwości wiążące.
2. Anionity (Wymieniacze anionowe)
Posiadają ładunek dodatni i wyłapują aniony (jony ujemne). Chromatografia z wykorzystaniem to tzw. Chromatografia anionowymymienna (AEX – Anion Exchange Chromatograhy). Podobnie jak CEX, tą też można podzielić na dwie kategorie:
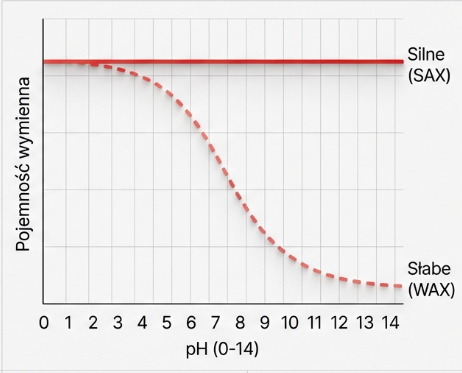
- Silne anionity (SAX – Strong Anion Exchange): Zazwyczaj oparte na czwartorzędowych solach amoniowych. Trzymają ładunek niezależnie od tego, czy pracujemy w środowisku kwaśnym, czy zasadowym.
- Słabe anionity (WAX – Weak Anion Exchange): Oparte na aminach trzeciorzędowych. Ich zdolność do wiązania maleje wraz ze wzrostem pH.
Wybór między anionitem a kationitem zależy od tego, jaki ładunek dominuje na Twojej cząsteczce w danych warunkach roboczych.
Zastosowanie chromatografii jonowymiennej
IEC w analityce: laboratoria środowiskowe
Laboratoria środowiskowe wykorzystują IEC (często nazywaną po prostu chromatografią jonową – IC) do oznaczania zawartości azotanów, siarczanów czy chlorków w wodzie pitnej. Systemy te wykrywają śladowe ilości zanieczyszczeń, które mogłyby zaszkodzić naszemu zdrowiu. Dzięki wysokiej czułości, chromatografy jonowe sprawdzają skład deszczówki, ścieków, a nawet napojów izotonicznych, które kupujesz w sklepie.
IEC w analityce: leki biotechnologiczne
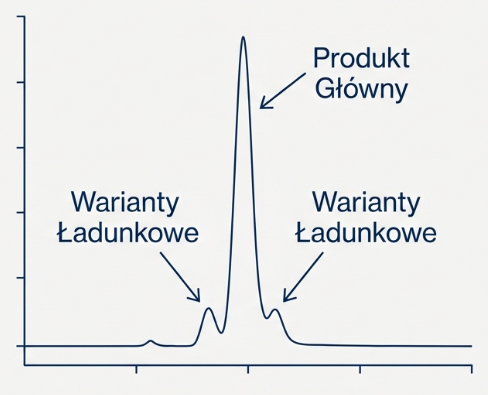
Chromatografia jonowymienna jest szeroko stosowana w laboratoriach kontroli jakości w firmach biotechnologicznych. Wykorzystuje się ją tam do określania poziomu wariantów ładunkowych produkowanego białka np. przeciwciał monoklonalnych czy insuliny. Jest to krytyczne z uwagi na fakt, że niektóre warianty ładunkowe mogą działać immunogennie lub wpływać na właściwości farmakologiczne leku.
IEC w preparatyce: Fabryka białek
W biotechnologii IEC to absolutny „koń pociągowy”. Gdy firma farmaceutyczna produkuje przeciwciała monoklonalne (stosowane np. w terapiach nowotworowych), musi oczyścić je z tysięcy białek gospodarza (komórek chomika lub bakterii).
Izolacja białek: Inżynierowie procesowi wykorzystują wielkie kolumny, które w jednym cyklu potrafią wyłapać kilogramy czystego terapeutyku.
Usuwanie kwasów nukleinowych: Ponieważ DNA i RNA mają silnie ujemny ładunek, anionity świetnie radzą sobie z ich usuwaniem z preparatów białkowych.
Jak zoptymalizować chromatografię jonowymienną?
Nawet najlepsza kolumna nie zadziała, jeśli nie zrozumiesz „charakteru” swojej próbki. Optymalizacja procesu to miejsce, gdzie chemia spotyka się z intuicją.
1. pH – Klucz do tożsamości
Białka to cząsteczki amfoteryczne – ich ładunek zależy od pH. Każde białko posiada punkt izoelektryczny (pI).
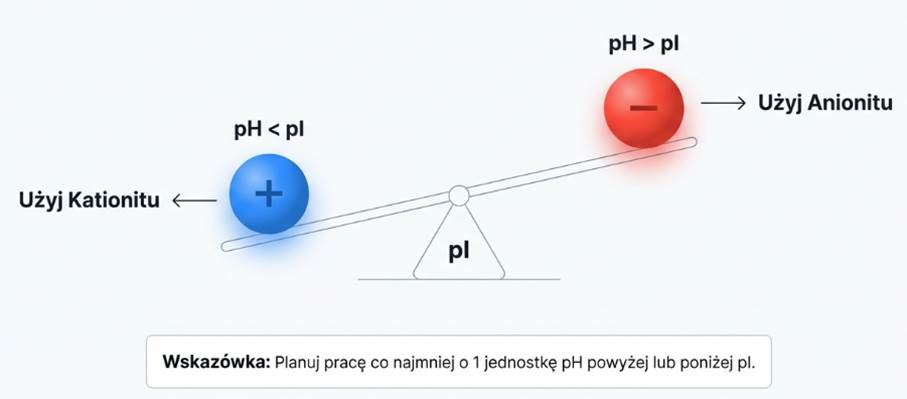
Przy pH poniżej pI, białko ma ładunek dodatni (użyj kationitu).
Przy pH powyżej pI, białko ma ładunek ujemny (użyj anionitu).
Pamiętaj o zasadzie „jednostki pH”: planuj pracę co najmniej o jedną jednostkę pH powyżej lub poniżej pI, aby zapewnić stabilne wiązanie.
2. Siła jonowa (Stężenie soli)
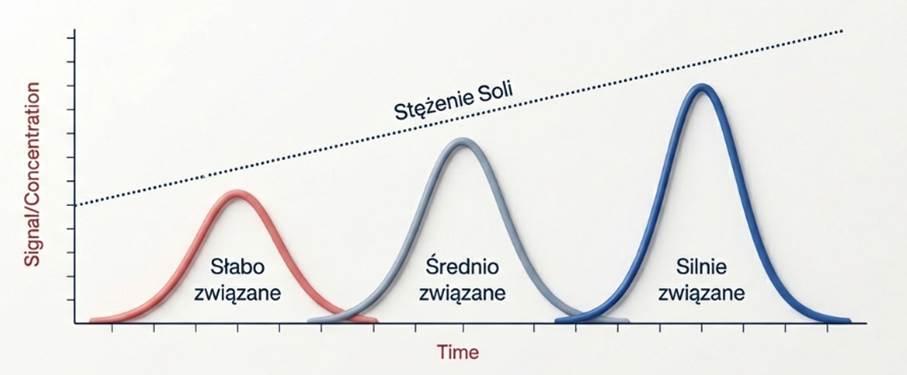
Sól to Twój główny gracz w etapie elucji. Zazwyczaj stosujemy gradient – powoli zwiększamy stężenie soli w buforze. Jony soli konkurują o miejsca wiązania z analitami. Im więcej jonów soli tym sprawniej wypychają analit z kolumny. Najsłabiej związane cząsteczki „odpadają” pierwsze, te najsilniejsze – na samym końcu. Precyzyjne sterowanie gradientem pozwala rozdzielić cząsteczki o niemal identycznym ładunku.
3. Prędkość przepływu i temperatura
Zbyt szybki przepływ sprawi, że cząsteczki nie zdążą „znaleźć” miejsca na złożu (zjawisko kinetyczne). Z kolei temperatura wpływa na lepkość buforu i stabilność delikatnych białek. Nowoczesne systemy FPLC (Fast Protein Liquid Chromatography) pozwalają monitorować te parametry w czasie rzeczywistym.
Podsumowanie
Chromatografia jonowymienna to potężne narzędzie, które łączy w sobie prostotę oddziaływań elektrostatycznych z niesamowitą precyzją rozdzielczą. Niezależnie od tego, czy analizujesz skład jonowy gleby, czy oczyszczasz kolejną generację leków biologicznych, zrozumienie mechanizmów IEC daje Ci przewagę w laboratorium.
Pamiętaj:
Ładunek to Twój kompas – dobierz złoże (anionit/kationit) do ładunku celu.
pH to Twój przełącznik – zmieniaj je, by kontrolować wiązanie białek.
Sól to Twój klucz – używaj jej, by uwalniać cząsteczki z kolumny w odpowiednim momencie.
Bibliografia i polecane źródła
Taylor T. (2012) Understanding Ion-Exchange Chromatography, LCGC North America
