
Technika RIA (Radioimmunoassay) jest najstarszą techniką immunochemiczną. Została opracowana przez Rosalyn Yalow i Solomona Bersona pod koniec lat 50-tych XX wieku. Zrewolucjonizowała pomiar stężenia hormonów we krwi, który do tej pory był niemal niewykonalnym zadaniem. Metoda radioimmunologiczna umożliwiło wykrycie substancji na poziomie pikogramów (10-12 g) a nawet femtogramów (10-15 g). Chociaż dziś wypierana jest przez nowsze, bezpieczniejsze techniki takie jak CLIA czy EMIT, RIA przez dekady była powszechnie stosowana w diagnostyce i endokrynologii. Za opracowanie metody radioimmunologicznej Rosalyn Yalow została uhonorowana nagrodą Nobla w 1977 roku. Solomon Berson zmarł w 1972 roku i niestety nie doczekał tego zaszczytu.

Co to jest technika RIA?
Metoda radioiimuologiczna (RIA) to niezwykle czuła technika analityczna in vitro, wykorzystująca reakcję swoistego wiązania antygenu z przeciwciałem oraz detekcję promieniowania jonizującego emitowanego przez radioizotopy. Jest to metoda zaliczana do grup metod kompetycyjnych (współzawodniczących).
U podstaw RIA leży wykorzystanie radioaktywnych znaczników (tracerów), które pozwalają na śledzenie losów cząsteczek biologicznych w układzie pomiarowym. Najczęściej stosowanym izotopem jest Jod-125 (125I), ze względu na korzystny okres półtrwania (ok. 60 dni) oraz wysoką aktywność właściwą, co przekłada się na czułość pomiaru.
Przed erą RIA, aby zbadać poziom insuliny, należało wykonywać skomplikowane testy na zwierzętach laboratoryjnych, co było mało precyzyjne i czasochłonne. RIA pozwoliła na wykonanie setek precyzyjnych testów w ciągu jednego dnia, bezpośrednio w próbkach surowicy pacjentów. Dziś RIA ustępuje nowszym i bezpieczniejszym technikom takim jak ELISA, CLIA czy EMIT. W dalszym ciągu jednak znajduje zastosowanie wszędzie tam, gdzie wymagana jest bardzo duża czułość np. w endokrynologii.
Mechanizm działania metody radioimmunologicznej
Fundamentem techniki RIA jest prawo działania mas oraz zjawisko konkurencji (kompetycji) o miejsca wiążące na przeciwciałach. Aby zrozumieć ten proces, musimy zdefiniować trzy kluczowe komponenty układu:
Antygen znakowany (Ag*): Znana ilość antygenu, do którego przyłączono atom radioizotopu.

Antygen nieznakowany (Ag): Substancja, której stężenie chcemy zmierzyć (np. insulina w surowicy pacjenta).

Swoiste przeciwciało (Ab): Białko wiążące dany antygen, dodawane w ilości ograniczonej (niedomiarowej) w stosunku do sumy antygenów.

Proces kompetycji
W mieszaninie reakcyjnej antygen znakowany i nieznakowany „walczą” o ograniczoną liczbę miejsc wiążących na przeciwciałach. Można to zapisać za pomocą równania:
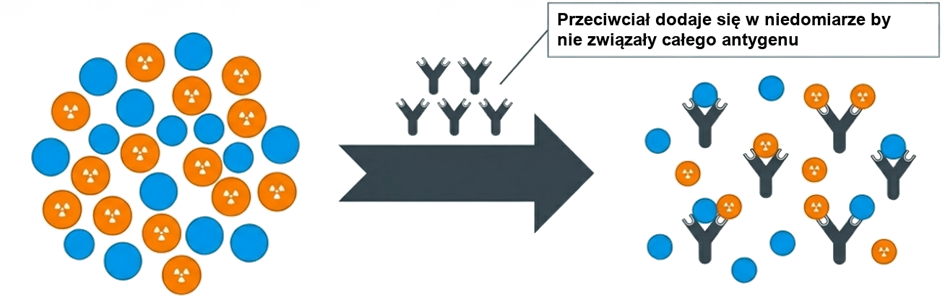
Im więcej antygenu nieznakowanego (z próbki pacjenta) znajduje się w roztworze, tym mniej antygenu znakowanego zdoła połączyć się z przeciwciałami. W efekcie, po osiągnięciu stanu równowagi, ilość radioaktywności związanej z przeciwciałami jest odwrotnie proporcjonalna do stężenia badanej substancji w próbce. Pomiaru dokonuje się w liczniku scyntylacyjnym – urządzeniu, który zlicza cząstki gamma emitowane przez znakowany antygen.

Rola powinowactwa i swoistości
Kluczem do sukcesu metody jest wysoka swoistość przeciwciała (zdolność do rozpoznawania tylko jednego, konkretnego epitopu) oraz jego powinowactwo (siła wiązania). Wysoka stała asocjacji przeciwciała pozwala na wykrywanie śladowych ilości analitu, co jest niemożliwe przy użyciu mniej precyzyjnych metod chemicznych.
Jak wykonać pomiar RIA?
Przeprowadzenie analizy RIA wymaga rygorystycznego przestrzegania procedur bezpieczeństwa radiologicznego oraz wysokiej precyzji pipetowania. Proces ten można podzielić na kilka etapów.
1. Przygotowanie odczynników i krzywej wzorcowej
Każde badanie musi zawierać krzywą wzorcową. Przygotowuje się serię probówek ze znanymi, wzrastającymi stężeniami standardu antygenu. Pozwala to później na odczytanie nieznanego stężenia z próbki pacjenta poprzez porównanie uzyskanej radioaktywności z wynikami standardów.
2. Inkubacja
Do probówek dodaje się stałą ilość antygenu znakowanego (Ag*) oraz stałą, ograniczoną ilość przeciwciał (Ab). Następnie dodaje się próbki badane lub standardy. Mieszanina jest inkubowana (często w temperaturze 4 °C lub temperaturze pokojowej przez kilka do kilkunastu godzin), aby umożliwić zajście reakcji antygen-przeciwciało i osiągnięcie stanu równowagi termodynamicznej.
3. Rozdział faz (Separacja)
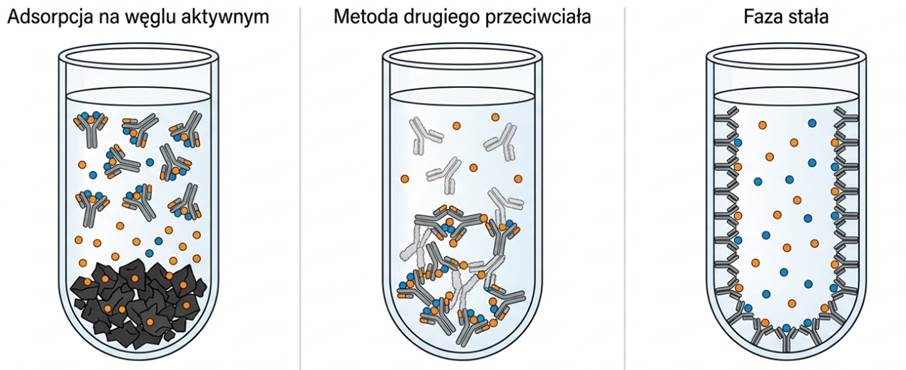
To najbardziej krytyczny etap RIA. Aby zmierzyć radioaktywność, musimy oddzielić frakcję związaną (kompleksy Ag-Ab i Ag*-Ab) od frakcji wolnej (niezwiązany Ag*). Stosuje się tu różne metody:
- Adsorpcja na węglu aktywnym: Węgiel pokryty dekstranem adsorbuje małe, wolne cząsteczki antygenu, pozostawiając duże kompleksy immunologiczne w roztworze.
- Metoda drugiego przeciwciała: Dodaje się drugie przeciwciało, które wiąże się z pierwszym (np. przeciwciało kozie przeciwko immunoglobulinom królika), powodując wytrącenie dużych agregatów.
- Faza stała: Przeciwciała są unieruchomione na ściankach probówki lub specjalnych kuleczkach magnetycznych, co ułatwia separację poprzez dekantację.
4. Pomiar radioaktywności i analiza wyników
Po rozdziale faz, mierzy się radioaktywność frakcji związanej za pomocą licznika scyntylacyjnego (w przypadku 125I). Stężenie odczytuje się z krzywej kalibracyjnej.
Wady i zalety techniki RIA
Mimo upływu lat i rozwoju metod alternatywnych, RIA wciąż zajmuje ważne miejsce w laboratoriach badawczych. Wybór tej metody zależy jednak od bilansu korzyści i ryzyk.
Zalety
- Wysoka czułość: Pozwala na wykrywanie cząsteczek w stężeniach, przy których testy ELISA często zawodzą (szczególnie w przypadku małych haptenów).
- Wysoka precyzja i powtarzalność: Metody radiometryczne są mniej podatne na błędy wynikające z obecności substancji interferujących w surowicy (np. barwników czy enzymów), które mogą zakłócać odczyty barwne w testach enzymatycznych.
- Mała objętość próbki: Do badania wystarcza zazwyczaj niewielka ilość materiału biologicznego.
Wady
- Zagrożenie radiacyjne: Praca z izotopami wymaga specjalistycznych uprawnień, monitoringu dawki promieniowania oraz rygorystycznych procedur bezpieczeństwa.
- Odpady radioaktywne: Generowanie trudnych i kosztownych w utylizacji odpadów.
- Krótki czas trwałości odczynników: Izotopy ulegają rozpadowi naturalnemu. Okres półtrwania 125I to 60 dni. W związku z tym odczynniki lub zestawy są ważne tylko przez około 2 miesiące. Jest to duże ograniczenie w porównaniu np. z testem ELISA, który nadaje się do użytku nawet przez kilka lat. W swojej karierze spotkałem się z przeciwciałami, które po 20 latach w zamrażarce dalej nadawały się do użytku.
- Koszt aparatury: Liczniki scyntylacyjne są drogim i specjalistycznym sprzętem, wymagającym regularnej kalibracji.
Zastosowanie techniki RIA
Yalow i Berson opracowali technikę RIA na potrzeby oznaczania insuliny. Jeszcze w latach 60-tych rozszerzyli zastosowanie metody na inne hormony. Przez dekady metoda radioiimunologiczna przyczyniła się do zbudowania wiedzy na temat regulacji hormonalnej ludzi i zwierząt. Jej zastosowanie nie ogranicza się jednak tylko do endokrynologii. Oto przykłady jej wykorzystania.
Endokrynologia
Oznaczanie
- Hormonów peptydowych: Insuliny, glukagonu, hormonu wzrostu (GH), parathormonu (PTH).
- Hormonów tarczycy: T3, T4 oraz TSH.
- Hormonów sterydowych: Kortyzolu, testosteronu, estradiolu i progesteronu. Dzięki RIA możliwe jest monitorowanie cyklu miesięcznego czy diagnostyka niedoczynności kory nadnerczy.
Onkologia i monitorowanie biomarkerów
RIA wykorzystuje się do oznaczania markerów nowotworowych, takich jak AFP (alfa-fetoproteina) czy CEA (antygen karcynoembrionalny). Wysoka czułość pozwala na wykrycie wznowy procesu nowotworowego na bardzo wczesnym etapie, gdy stężenie markerów w krążeniu jest jeszcze znikome.
Farmakologia i Toksykologia
Oznaczanie poziomu leków o wąskim oknie terapeutycznym (np. digoksyny, leków immunosupresyjnych czy przeciwpadaczkowych) jest kluczowe dla bezpieczeństwa pacjenta. RIA pozwala na precyzyjne monitorowanie stężenia terapeutycznego leku w surowicy. Obecnie jest coraz częściej wypierana przez analizy LC-MS/MS.
Badania naukowe
W laboratoriach biochemicznych RIA służy do badania dynamiki interakcji receptor-ligand oraz w badaniach nad nowymi lekami, gdzie konieczne jest śledzenie losów substancji w układach komórkowych.
Podsumowanie
Technika radioimmunologiczna, choć liczy sobie już ponad sześć dekad, pozostaje jednym z najbardziej eleganckich i precyzyjnych narzędzi w arsenale biologa molekularnego i diagnosty. Jej wprowadzenie pozwoliło na zrozumienie działania układu endokrynnego i fizjologii człowieka i zwierząt.
Dziś wypierana jest przez nowsze techniki takie jak ELISA, EMIT czy CLIA. Mimo tego, w dalszym ciągu znajduje zastosowanie wszędzie tam, gdzie wymagana jest bardzo duża czułość.
Bibliografia
- Goldsmith, S. J. (1975). 'Radioimmunoassay: Review of Basic Principles’, Seminars in Nuclear Medicine, 5(2), pp. 125-152.
- Wild, D. (2013). The Immunoassay Handbook: Theory and Applications of Ligand Binding, ELISA and Related Techniques. 4th edn. Oxford: Elsevier.
- Yalow, R. S. and Berson, S. A. (1960). 'Immunoassay of endogenous plasma insulin in man’, Journal of Clinical Investigation, 39(7), pp. 1157-1175.
- Zimmerman, H. J. (red.) (2001). Principles and Practice of Immunoassay. 2nd edn. New York: Stockton Press.
- https://www.sciencehistory.org/education/scientific-biographies/rosalyn-yalow-and-solomon-berson/
Grafika:
- Okładka wygenerowana przez AI
- Grafika własna
- Sciencehistory.org
Często zadawane pytania (FAQ)
Jod-125 jest niemal idealnym znacznikiem w RIA z trzech powodów:
Posiada stosunkowo długi okres półtrwania (ok. 60 dni), co pozwala na transport i przechowywanie zestawów testowych.
Emituje promieniowanie gamma o niskiej energii, które jest łatwe do wykrycia przez liczniki, a jednocześnie relatywnie proste do osłonięcia (bezpieczeństwo pracy).
Chemicznie łatwo przyłącza się do reszt tyrozynowych w białkach, nie niszcząc ich struktury i właściwości biologicznych.
Tak, jak w każdej metodzie immunochemicznej. Najczęstszą przyczyną są przeciwciała heterofilne obecne w surowicy pacjenta (np. u osób mających częsty kontakt ze zwierzętami), które mogą nieswoiście wiązać się z odczynnikami testowymi. Innym powodem mogą być błędy techniczne na etapie separacji frakcji wolnej od związanej – niedokładne wypłukanie niezwiązanego izotopu zawsze zafałszuje wynik.
Laboratorium musi posiadać specjalne zezwolenie od krajowej agencji atomistyki (w Polsce PAA). Wymagane są: wydzielona strefa pracy izotopowej, system monitorowania skażeń, specjalistyczne liczniki gamma oraz rygorystyczne procedury utylizacji odpadów promieniotwórczych. Ze względu na te koszty, mniejsze placówki zazwyczaj zlecają takie badania laboratoriom referencyjnym.
