Chyba każdy w życiu spotkał się z testem paskowym. Sprzedawane na potęgę testy ciążowe, testy na obecność wirusów czy narkotyków, wykorzystują ten sam niesamowity mechanizm. Są nim przeciwciała. Przeciwciała naturalnie występują u zwierząt i umożliwiają im uodparnianie się na niebezpieczne patogeny (w szczególności wirusy i bakterie). Czasami stwarzają problemy i są źródłem alergii. Biolodzy i biotechnolodzy nauczyli się wykorzystywać przeciwciała do swoich celów. Wykorzystuje się je jako niezwykle skuteczne leki. W laboratorium pełnią funkcję wysoko specyficznych detektorów. Dziedzina analityczna wykorzystująca przeciwciała to tzw. Immunochemia. Obecnie mamy szeroki wachlarz metod immunochemicznych wykorzystywanych w różnych celach.

Czym jest immunochemia?
Immunochemia analityczna zajmuje się ilościowym oznaczaniem substancji (analitów) przy wykorzystaniu specyficznej reakcji wiązania między antygenem a przeciwciałem.
Kluczowym pojęciem jest tutaj immunoanaliza (ang. immunoassay). Jest to metoda bioanalityczna, w której swoistość przeciwciała względem antygenu służy jako mechanizm selekcji, natomiast zastosowany znacznik (np. enzym, izotop, luminofor) pozwala na przekształcenie tego biologicznego zdarzenia w mierzalny sygnał fizyczny lub chemiczny.
W immunchemiii dążymy do osiągnięcia dwóch parametrów krytycznych:
- Czułość analityczna: zdolność do wykrywania minimalnych ilości analitu.
- Swoistość (specyficzność): zdolność do odróżnienia badanego analitu od innych, strukturalnie podobnych cząsteczek obecnych w matrycy (np. w surowicy krwi).
Przeciwciała jako narzędzia analityczne
Fundamentem każdej metody immunochemicznej jest przeciwciało (immunoglobulina, Ig). W naturze są to białka efektorowe układu odpornościowego, produkowane przez limfocyty B. W laboratorium są niezwykle specyficznymi ligandami, które działają jak swego rodzaju detektory.
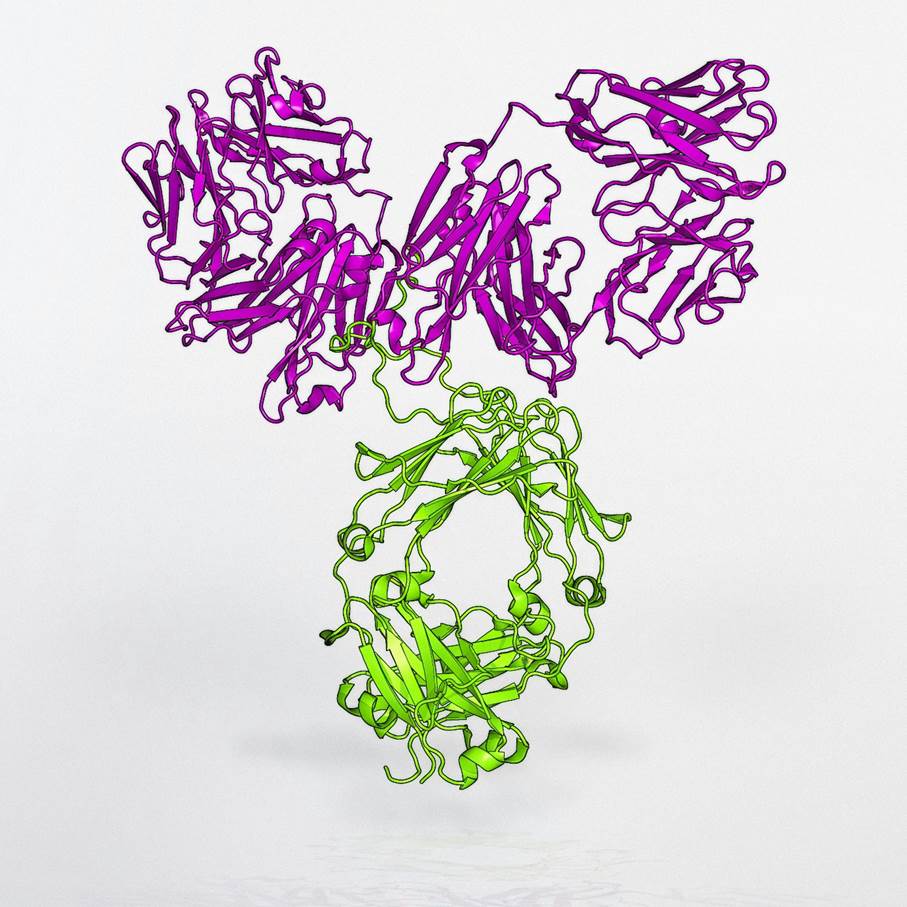
Struktura i funkcjonalność przeciwciał
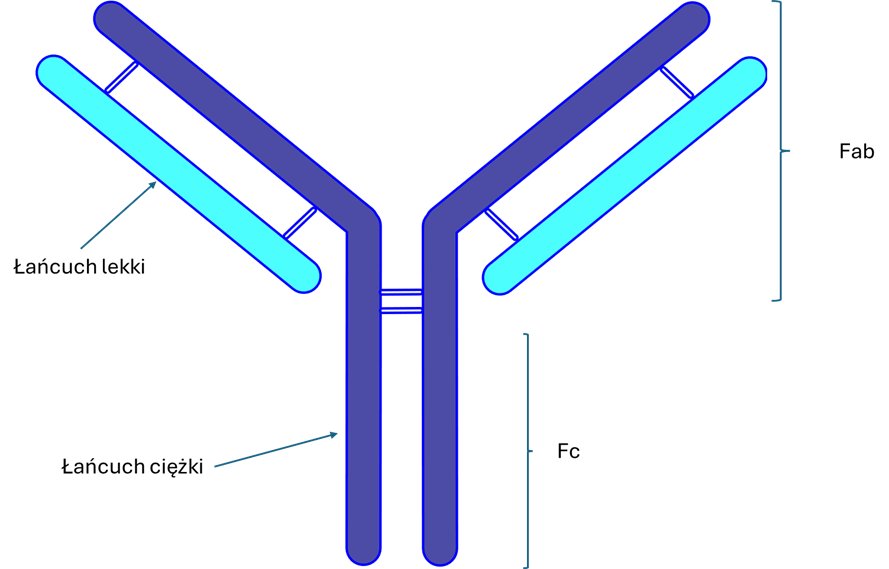
W immunochemii najczęściej stosuje się przeciwciała klasy IgG. Składają się one z dwóch łańcuchów ciężkich (H) i dwóch lekkich (L). Ponadto wyróżnić można fragmenty Fab (wiążący antygen i Fc (region kosnerwatywny). To właśnie fragment Fab, który zawiera regiony hiperzmienne odpowiada za wiązanie antygenów (analitów lub ich fragmentów). Fragment Fc w naturze odpowiada za wiązanie przeciwciała z receptorami na powierzchni komórek.
Oto wyjaśnienie kilku terminów związanych z budową przeciwciał i zasadą ich działania
Fab (Fragment antygen – binding) – Fragment wiążący antigen. Jest to część przeciwciała, która zawiera regiony hiperzmienne. Rozpoznają one epitop antygenu i wiążą go. W skład Fab wchodzą oba łańcuchy lekkie i część łańcucha ciężkiego
Fc (Fragment conservative) – konserwatywny region przeciwciała, którego sekwencja nie zmienia się. Odpowiada za wiązanie przeciwciała z jego receptorem na powierzchni komórek np. limfocytów T.
Antygen – substancja obca rozpoznawana przez przeciwciało. Może to być cząsteczka wirusa, białka bakterii, Lipopolisacharyd, alergeny.
Epitop – fragment antygenu, które jest rozpoznawane przez przeciwciało. Jeden antygen może mieć kilka epitopów.
Paratop – część regionu Fab zawierające hiperzmienne regiony i biorące udział w wiązaniu epitopu.
Powinowactwo i zachłanność
Skuteczność pomiaru zależy od dwóch parametrów termodynamicznych:
- Powinowactwo (afinitet): siła wiązania między pojedynczym paratopem a pojedynczym epitopem. Opisywane jest przez stałą dysocjacji ($K_d$). Im niższa wartość $K_d$, tym silniejsze wiązanie i wyższa czułość testu.
- Zachłanność (awidność): łączna siła wiązania wielowartościowego. Ponieważ przeciwciała IgG mają dwa miejsca wiążące, mogą wiązać się z dwoma epitopami jednocześnie, co drastycznie zwiększa stabilność kompleksu.
W immunochemii wykorzystujemy dwa rodzaje przeciwciał:
- Poliklonalne: mieszanina przeciwciał rozpoznających różne epitopy na tym samym antygenie. Są łatwiejsze w produkcji, ale mogą wykazywać reaktywność krzyżową.
- Monoklonalne: identyczne cząsteczki rozpoznające jeden, konkretny epitop. Zapewniają najwyższą powtarzalność i swoistość pomiaru.
Przegląd metod immunochemicznych
Pierwsze metody immunochemiczne wprowadzono w latach 50 XX wieku. I choć wykorzystują ten sam biologiczny mechanizm to obecnie jest ich cała gama.
RIA (Radioimmunoassay)
Wprowadzona w latach 50. XX wieku przez Rosalyn Yalow (za co otrzymała Nagrodę Nobla), metoda RIA wykorzystuje izotopy promieniotwórcze (np.I125) jako znaczniki. Choć niezwykle czuła, obecnie jest wypierana ze względu na ryzyko radiologiczne i krótki czas półtrwania izotopów.
ELISA (Enzyme-Linked Immunosorbent Assay)
Metoda immunoenzymatyczna, w której znacznikiem jest enzym (np. peroksydaza chrzanowa – HRP). Po dodaniu substratu, enzym katalizuje reakcję barwną, której intensywność (absorbancja) jest proporcjonalna do ilości analitu.

CLIA (Chemiluminescence Immunoassay)
Obecnie dominująca technika w dużych analizatorach laboratoryjnych. Znacznikiem są cząsteczki zdolne do emisji światła w wyniku reakcji chemicznej (np. estry akrydyny). CLIA oferuje znacznie szerszy zakres dynamiki i niższą granicę wykrywalności niż ELISA.
Western – blot
Jest to technika, w której wykorzystuje się przeciwciała do wykrywania białek rozdzielonych wcześniej elektroforetycznie np. w SDS – Page. Białka przenosi się z żelu na membranę. Przeciwciała wiążą specyficzne białka. Metoda wykorzystuje najczęściej znaczniki barwne lub fluorescencyjne. Western blot wykorzystywany jest często do badania ekspresji genów.
EMIT
Enzyme Multiplied Immunoassay Technique. Zasada działania tej techniki opiera się na konkurencji i modulacji aktywności enzymu przez przeciwciało. W metodzie używa się specyficznych przeciwciał oraz anality znakowanego enzymem (koniugatu). Analit z próbki współzawodniczy z koniugatem o przeciwciało. Im więcej analitu w próbce tym mniej koniugatu połączy się z przeciwciałem. Po złączeniu koniugatu z przeciwciałem dochodzi do inhibicji działania enzymu. Im więcej analitu znajduje się w próbce tym więcej enzymu jest aktywne a sygnał jest silniejszy. Metoda jest szybka. Nie wymaga absorpcji przeciwciał lub próbki na powierzchni płytki i oddzielania frakcji związanej od wolnej. Z tego powodu jest często wykorzystywana w automatycznych analizatorach
Immunochromatografia
Immunochromatografia jest techniką przystosowaną do wykorzystania w warunkach domowych. Próbkę nanosi się na bibułę. Siły kapilarne powoduję ruch próbki przez bibułę. Przeciwciała wiążą zawarte w próbce antygeny a wynik najczęściej widoczny jest w postaci barwnych pasków. W ten sposób działają właśnie paskowe testy dostępne w każdej aptece (testy ciążowe, testy na obecność Covid-19, testy PSA).
Metody homogenne vs heterogenne
Ważnym podziałem technicznym jest konieczność oddzielania frakcji wolnej od związanej:
- Metody heterogenne (np. ELISA): Wymagają etapów płukania, aby usunąć niezwiązane przeciwciała. Są czulsze.
- Metody homogenne (np. EMIT): Pomiar następuje bezpośrednio w mieszaninie reakcyjnej bez płukania. Są szybsze, idealne do oznaczania leków w stanach nagłych.
Zastosowania immunochemii
Diagnostyka kliniczna i endokrynologia
To tutaj immunochemia jest najczęściej stosowana. Oznaczanie hormonów tarczycy (TSH, fT4), hormonów płciowych czy markerów metabolizmu kostnego opiera się niemal wyłącznie na technikach immunochemicznych. Precyzja tych pomiarów pozwala na wykrywanie subklinicznych postaci chorób.
Wykrywanie markerów nowotworowych takich jak PSA (rak prostaty), AFP (rak wątroby) czy CA-125 (rak jajnika) opiera się na metodach immunometrycznych. Choć rzadko służą one do samodzielnego stawiania diagnozy, są kluczowe w monitorowaniu skuteczności leczenia i wykrywaniu wczesnych nawrotów.
Oznaczanie troponin sercowych (cTnI, cTnT) metodami wysokoczułej immunometrii (hs-cTn) uratowało tysiące istnień, pozwalając na błyskawiczne wykluczenie lub potwierdzenie zawału mięśnia sercowego w warunkach szpitalnego oddziału ratunkowego.
Monitorowanie Terapii Monitorowanej (TDM)
U pacjentów przyjmujących leki o wąskim oknie terapeutycznym (np. digoksyna, leki immunosupresyjne, przeciwpadaczkowe), immunochemia pozwala na bieżąco korygować dawkę, zapobiegając toksyczności.
Testy Point-of-Care (POCT)
Szybkie testy antygenowe (np. na grypę, RSV czy COVID-19) oraz domowe testy ciążowe to w rzeczywistości uproszczona immunochromatografia.
Wyzwania i pułapki analityczne
Mimo swojej potęgi, immunochemia nie jest wolna od wad. Doświadczony diagnosta musi brać pod uwagę zjawiska takie jak:
- Efekt haka (hook effect): Przy ekstremalnie wysokich stężeniach analitu sygnał paradoksalnie spada, co może prowadzić do fałszywie niskich wyników.
- Przeciwciała heterofilne: Obecne w surowicy pacjenta przeciwciała (np. po kontakcie ze zwierzętami) mogą nieswoiście wiązać się z odczynnikami testowymi, dając wyniki fałszywie dodatnie.
- Reaktywność krzyżowa: Gdy przeciwciało rozpoznaje cząsteczkę o strukturze zbliżonej do badanego analitu (np. metabolity leków).
Podsumowanie
Immunochemia pokazuje jak doskonale człowiek wykorzystuje naturalne mechanizmy biologiczne. Dziś techniki immunochemiczne ratują życie milionom pacjentów poprzez wspomaganie diagnostyki i procesu rozwoju leków.
Bibliografia
- Wild, D. (red.) (2013). The Immunoassay Handbook: Theory and Applications of Ligand Binding, ELISA and Related Techniques. Elsevier Science.
- Crowther J. R. (2000). The ELISA guidebook. Methods in molecular biology (Clifton, N.J.), 149, III–413.
- Howanitz JH. Immunoassay. Innovations in label technology. Arch Pathol Lab Med. 1988;112(8):775-779.
Grafika
- Grafika własna
- Photo by Roman Wimmers on Unsplash
- Photo by National Institute of Allergy and Infectious Diseases on Unsplash
FAQ
To zjawisko występuje w testach typu „kanapkowego” (sandwich), gdy stężenie analitu w próbce jest ekstremalnie wysokie. Nadmiar antygenu nasyca zarówno przeciwciała chwytające na podłożu, jak i przeciwciała znakowane w roztworze, uniemożliwiając im utworzenie kompleksu „kanapkowego”. W rezultacie, mimo ogromnej ilości substancji, aparat odczytuje bardzo niski sygnał. Może to prowadzić do tragicznych w skutkach pomyłek diagnostycznych, np. błędnego wyniku poziomu markerów nowotworowych. By rozwiązać ten problem można stosować seryjne rozcieńczenia próbek np. testowanie 3 różnych rozcieńczeń.
Przeciwciała monoklonalne są produktem jednego klonu limfocytów B, co oznacza, że każda cząsteczka w partii jest identyczna i rozpoznaje ten sam, konkretny epitop. Zapewnia to doskonałą powtarzalność testów i minimalizuje ryzyko reaktywności krzyżowej. Przeciwciała poliklonalne, będąc mieszaniną różnych immunoglobulin, mogą wiązać się z różnymi fragmentami antygenu, co zwiększa sygnał (czułość), ale kosztem precyzji i powtarzalności.
Tak, większość szybkich testów kasetkowych (np. na obecność THC czy morfiny w moczu) wykorzystuje metodę immunochromatografii. Zaletą tej techniki jest szybkość. Wadą jest brak odpowiedzi ilościowej. W celu ilościowego oznaczenia narkotyków konieczne sa testy laboratoryjne.
Przeciwciała heterofilne to endogenne przeciwciała obecne w osoczu pacjenta. Mogą one „skleić” przeciwciało chwytające z wykrywającym nawet pod nieobecność analitu, co daje wynik fałszywie dodatni. Jest to jedno z największych wyzwań w nowoczesnej diagnostyce immunochemicznej. Jeśli organizm wytwarza przeciwciała przeciwko analitowi mogą one uniemożliwić wychwyt analitu przez przeciwciała wykorzystywane w teście.
Główną przewagą CLIA jest szeroki zakres dynamiki pomiaru oraz niższa granica wykrywalności. Chemiluminescencja generuje sygnał świetlny na „czarnym tle”, co pozwala wykryć nawet pojedyncze cząsteczki analitu. Ponadto testy CLIA są w pełni zautomatyzowane, a czas uzyskania wyniku jest znacznie krótszy (nawet 15–30 minut) w porównaniu do kilku godzin w przypadku klasycznej płytki ELISA.
Tak, choć wymaga to zastosowania formatu kompetencyjnego. Małe cząsteczki (hapteny) są zbyt małe, by zostać jednocześnie związane przez dwa przeciwciała (wymagane w metodzie kanapkowej). W teście kompetencyjnym (np. EMIT) antygen z próbki rywalizuje ze znakowanym antygenem o ograniczoną liczbę miejsc wiążących na przeciwciałach. Im więcej leku w próbce pacjenta, tym mniej znakowanego antygenu zostanie związane.
