W dzisiejszej biologii molekularnej trudno wyobrazić sobie narzędzie bardziej wszechstronne, czułe i niezbędne niż qPCR (quantitative Polymerase Chain Reaction). Od diagnozowania infekcji wirusowych w skali globalnej, przez badanie ekspresji genów w nowotworach, aż po analizę jakości żywności – qPCR (lub inaczej Real-Time PCR) ta stała się złotym standardem nowoczesnej analityki.

Od PCR do qPCR
Klasyczna metoda PCR, opracowana w latach 80. przez Kary’ego Mullisa, zrewolucjonizowała naukę, umożliwiając selektywne powielanie fragmentów DNA. Miała ona jednak istotne ograniczenie: była metodą end-point (punktu końcowego). Oznaczało to, że badacz mógł ocenić wynik dopiero po zakończeniu wszystkich cykli, zazwyczaj za pomocą elektroforezy żelowej. Metoda ta pozwalała stwierdzić obecność genu, ale nie jego pierwotną ilość.
qPCR (ilościowy PCR), znany również jako Real-Time PCR, umożliwia monitorowanie przyrostu produktu w trakcie trwania reakcji, w każdym jej cyklu. Dzięki wykorzystaniu znaczników fluorescencyjnych, intensywność sygnału świetlnego jest proporcjonalna do ilości powstałego DNA. Pozwala to na precyzyjne określenie, ile cząsteczek matrycy znajdowało się w próbie wyjściowej.
Jak działa qPCR?
Fundamentem qPCR jest zdolność do przekształcenia chemicznej syntezy DNA w mierzalny sygnał fizyczny. Obecnie stosuje się dwie główne strategie detekcji:
Barwniki interkalujące (np. SYBR Green I)
To rozwiązanie najbardziej ekonomiczne i uniwersalne. Barwnik SYBR Green wiąże się niespecyficznie z każdą dwuniciową cząsteczką DNA (dsDNA). W stanie wolnym wykazuje minimalną fluorescencję, która drastycznie wzrasta po związaniu się z małą bruzdą helisy DNA.
- Zaleta: Brak konieczności projektowania specyficznych sond dla każdego genu.
- Wada: Niska specyficzność – barwnik świeci również w obecności dimerów starterów lub produktów niespecyficznych. Aby potwierdzić wiarygodność, niezbędna jest analiza krzywej topnienia (melting curve).
Sondy hydrolizujące (np. TaqMan)
Metoda ta opiera się na zjawisku FRET (Förster Resonance Energy Transfer). Sonda to krótki odcinek DNA komplementarny do fragmentu wewnątrz powielanej sekwencji, znakowany na końcach dwoma cząsteczkami:
- Reporterem (R): Fluorofor emitujący światło.
- Wygaszaczem (Quencher, Q): Absorbuje energię z reportera, dopóki ten jest w bliskim sąsiedztwie.
Podczas elongacji, polimeraza DNA (posiadająca aktywność 5′-3′ egzonukleazy) napotyka sondę i ją degraduje. Uwolniony reporter oddala się od wygaszacza, co skutkuje emisją mierzalnego sygnału fluorescencyjnego.
- Zaleta: Ekstremalnie wysoka specyficzność i możliwość multipleksowania (wykrywania kilku genów w jednej probówce dzięki różnym kolorom reporterów).
Anatomia krzywej amplifikacji i cykl progowy (Cq)
Wynikiem reakcji qPCR jest wykres przedstawiający zależność natężenia fluorescencji od numeru cyklu. Typowa krzywa ma kształt sigmoidalny i dzieli się na fazy:
- Faza bazowa (Background): Fluorescencja jest poniżej progu detekcji urządzenia.
- Faza wykładnicza (Exponential): Następuje podwojenie produktu w każdym cyklu (przy 100% wydajności). To tutaj wykonuje się pomiary.
- Faza liniowa: Składniki reakcji (dNTPs, startery) zaczynają się wyczerpywać.
- Faza plateau: Reakcja ustaje, brak dalszego przyrostu sygnału.
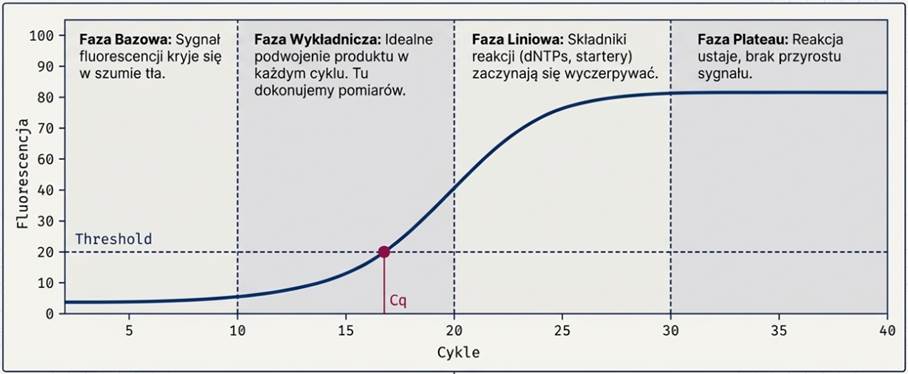
Parametrem który jest używany do oznaczenia ilościowego jest jest Cq (Quantification Cycle – cykl oznaczalności). Można się też spotkać z nazwą Cy – (threshold Cycle – cykl progowy). Jest to cykl, w którym sygnał fluorescencji przekracza linię progu (threshold) i staje się istotny statystycznie ponad szum tła.
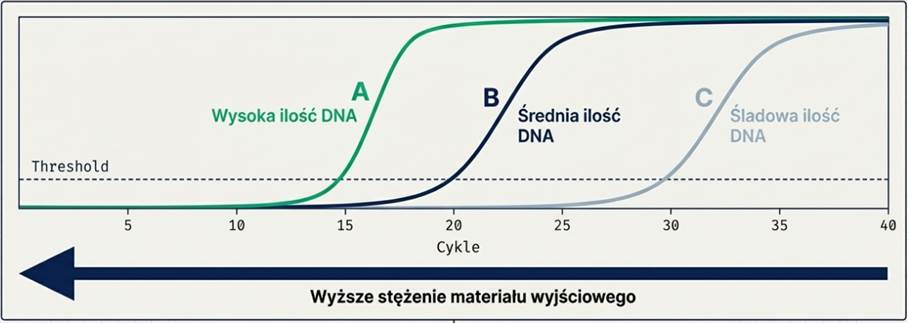
Zależność matematyczna: Im więcej matrycy DNA w próbie wyjściowej, tym wcześniej następuje wzrost fluorescencji i tym niższa jest wartość Cq.
Strategie kwantyfikacji
Wykonując qPCR możesz wybrać dwa podejścia do oznaczania ilościowego swoich próbek.
Kwantyfikacja bezwzględna (Absolute Quantification)
Stosowana, gdy musimy znać dokładną liczbę kopii DNA w próbie (np. miano wirusa we krwi). Wymaga przygotowania krzywej wzorcowej z użyciem seryjnych rozcieńczeń standardu o znanym stężeniu. Porównując Cq próbki badanej z krzywą wzorcową, odczytujemy konkretną liczbę cząsteczek. Ta strategia jest często wykorzystywana w laboratoriach diagnostycznych lub laboratoriach kontroli jakości. Przykładem może być np. oznaczanie ilościowe pozostałości DNA bakterii w leku biologicznym. Analiza wymaga wzorca DNA bakterii, która była wykorzystywana do produkcji leku.
Kwantyfikacja względna (Relative Quantification)
Najczęściej stosowana w badaniach ekspresji genów. Nie interesuje nas liczba kopii, ale zmiana poziomu mRNA w grupie badanej (np. po podaniu leku) względem grupy kontrolnej. Aby zniwelować błędy pipetowania i różnice w jakości RNA, stosuje się geny referencyjne (tzw. housekeeping genes, np. GAPDH, ACTB), których poziom w komórce jest stały.
Najpopularniejszą metodą obliczeniową jest wzór Livaka
W celu wykazania różnicy pomiędzy grupą badaną a kontrolną stosuje się następujący wzór.
Wynik wskazuje krotność zmiany (fold change) poziomu ekspresji badanego genu.
Zastosowania qPCR
Wszechstronność qPCR sprawia, że jest to technika obecna niemal w każdej dziedzinie nauk o życiu:
- Diagnostyka medyczna: Wykrywanie patogenów (wirusów HIV, HCV, SARS-CoV-2, bakterii Mycobacterium tuberculosis). qPCR pozwala na szybką identyfikację nawet przy niskim mianie patogenu.
- Onkologia: Monitorowanie minimalnej choroby resztkowej oraz ocena poziomu nadekspresji onkogenów (np. HER2 w raku piersi), co determinuje wybór terapii celowanej.
- Genetyka sądowa: Ilościowe oznaczanie DNA ludzkiego w zabezpieczonych śladach biologicznych przed przystąpieniem do profilowania STR.
- Badanie żywności: Wykrywanie organizmów modyfikowanych genetycznie (GMO) oraz identyfikacja alergenów lub zafałszowań składu (np. obecność koniny w produktach wołowych).
- Ekologia molekularna: Analiza eDNA (environmental DNA) pozwala na monitorowanie rzadkich gatunków zwierząt w zbiornikach wodnych jedynie na podstawie fragmentów DNA pozostawionych w wodzie.
- Biotechnologia: Analiza pozostałości DNA hosta w lekach biotechnologicznych (białkach rekombinowanych takich jak insulina czy przeciwciała monoklonalne)
Dobre praktyki i kontrola jakości (Wytyczne MIQE)
Aby wyniki qPCR były wiarygodne i powtarzalne, społeczność naukowa opracowała wytyczne MIQE (Minimum Information for Publication of Quantitative Real-Time PCR Experiments). Do najważniejszych aspektów należą:
- Wydajność reakcji (E): Powinna mieścić się w zakresie 90–110%. Idealna wydajność (E=2) oznacza, że ilość DNA podwaja się dokładnie co cykl.
- Czystość matrycy: Zanieczyszczenia chemiczne (np. fenol, etanol, sole) mogą inhibować polimerazę, sztucznie zawyżając wartości Cq.
- Kontrole negatywne (NTC): Próba bez matrycy DNA pozwala wykluczyć kontaminację odczynników.
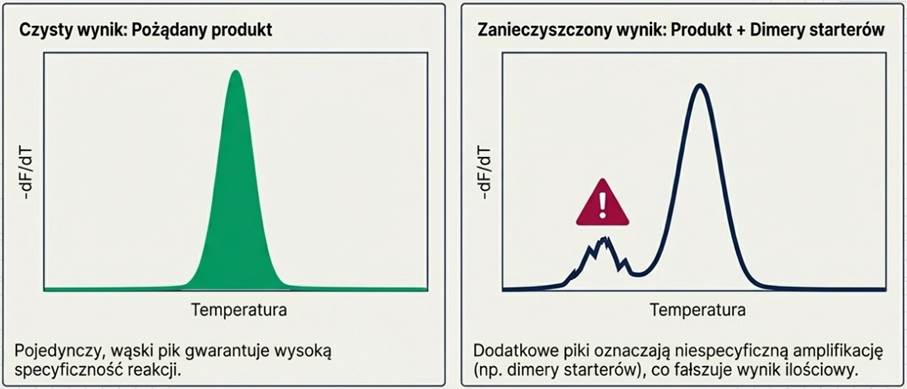
- Analiza krzywej topnienia: W przypadku SYBR Green, pojedynczy, wąski pik na wykresie pochodnej fluorescencji względem temperatury gwarantuje, że powielany jest tylko jeden, właściwy produkt (metoda jest specyficzna).
Podsumowanie
Metoda qPCR to potężne narzędzie, które przekształciło biologię z nauki opisowej w precyzyjną dyscyplinę ilościową. Choć na poziomie technicznym opiera się na prostym zjawisku fluorescencji i enzymatycznej syntezie DNA, jej prawidłowe wykorzystanie wymaga głębokiego zrozumienia kinetyki reakcji oraz rygorystycznej analizy danych. W dobie medycyny personalizowanej i rosnących zagrożeń epidemiologicznych, rola qPCR będzie tylko wzrastać, stanowiąc fundament nowoczesnej bioanalityki.
Bibliografia:
- Bustin, S. A., et al. (2009). The MIQE guidelines: Minimum information for publication of quantitative real-time PCR experiments. Clinical Chemistry, 55(4), 611-622.
- Higuchi, R., Fockler, C., Dollinger, G., & Watson, R. (1993). Kinetic PCR analysis: Real-time monitoring of DNA amplification reactions. Bio/Technology, 11(9), 1026-1030.
- Kubista, M., et al. (2006). The real-time polymerase chain reaction. Molecular Aspects of Medicine, 27(2-3), 95-125.
- Livak, K. J., & Schmittgen, T. D. (2001). Analysis of relative gene expression data using real-time quantitative PCR and the 2−ΔΔCT method. Methods, 25(4), 402-408.
- Pfaffl, M. W. (2001). A new mathematical model for relative quantification in real-time RT-PCR. Nucleic Acids Research, 29(9), e45.
