W poprzednim artykule pisałem o rodzajach detektorów w HPLC. Istnieje cała gama różnych opcji do wyboru. Nie zawsze jednak laboratorium tym wyborem dysponuje. Większość posiada po prostu detektor UV-VIS. Co wtedy? Czy jest jakiś sposób by wykryć niewidzialne dla tego detektora związki? Oczywiście! Wystarczy te związki zmienić chemicznie tak by stały się widzialne. Ta chemiczna zmiana analitu to właśnie derywatyzacja. Wykrycie niewidzialnego to jedynie jedno z jej zastosowań. Jakie są inne? Jak ją wykonać? Tego dowiesz się z poniższego tekstu.
Czym jest derywatyzacja w HPLC?
W kontekście chromatografii cieczowej, derywatyzacja to proces chemicznego przekształcenia analitu w produkt o zmienionych właściwościach fizykochemicznych, zwany pochodną (deriwatem). Reakcja ta zachodzi zwykle pomiędzy specyficzną grupą funkcyjną cząsteczki a dobranym odczynnikiem derywatyzującym.
Kluczowym aspektem derywatyzacji jest jej ilościowy charakter. Idealna reakcja powinna być szybka, selektywna, zachodzić ze 100% wydajnością i prowadzić do powstania jednego, stabilnego produktu, który nie ulega rozkładowi w warunkach prowadzenia analizy.
Po co robić derywatyzację?
Wiele cząsteczek o znaczeniu biologicznym (np. aminokwasy, cukry, małe kwasy organiczne) nie posiada chromoforów ani fluoroforów. Z tego powodu są one niewidoczne dla detektorów, które standardowo znajdują się na wyposażeniu laboratoriów. Derywatyzacja rozwiązuje ten problem, realizując trzy główne cele:

A. Poprawa detekcji (Czułość i Selektywność)
Większość rutynowych laboratoriów opiera się na detektorach UV-Vis lub fluorescencyjnych (FLD). Jeśli analit nie absorbuje światła w zakresie powyżej 210 nm, jego detekcja jest utrudniona przez szum tła rozpuszczalników. Wprowadzenie do cząsteczki grupy o wysokim molowym współczynniku absorpcji (np. grupy dabsylowej) lub zdolności do fluorescencji (np. grupy dansylowej) pozwala na drastyczne zwiększenie czułości.
B. Zmiana właściwości chromatograficznych (Retencja i Rozdzielczość)
Cząsteczki bardzo polarne, takie jak krótkołańcuchowe kwasy alifatyczne, często eluują w pobliżu czasu martwego kolumn typu C18. Derywatyzacja pozwala na „zamaskowanie” grup polarnych i wprowadzenie fragmentów hydrofobowych, co zwiększa retencję i umożliwia lepszą separację od składników matrycy.
C. Stabilizacja analitów
Niektóre związki są nietrwałe w warunkach chromatograficznych. Przekształcenie ich w stabilne pochodne (np. derywatyzacja grup tiolowych) zapobiega ich utlenianiu lub degradacji na kolumnie.
Kiedy wykonać derywatyzację
Wybór momentu przeprowadzenia reakcji chemicznej ma fundamentalny wpływ na konstrukcję układu pomiarowego oraz jakość uzyskiwanych wyników.
Derywatyzacja przedkolumnowa (Pre-column)
Proces ten zachodzi przed nastrzykiem próbki na kolumnę chromatograficzną. Może być realizowany manualnie (np. podczas przygotowania próbki) lub automatycznie przez robota dozującego (autosampler).
- Zalety:
- Brak ograniczeń czasowych dla wolnych reakcji.
- Możliwość usunięcia nadmiaru odczynnika (np. poprzez ekstrakcję lub odparowanie), co chroni kolumnę.
- Możliwość zastosowania drastycznych warunków (wysoka temperatura, pH).
- Brak dodatkowego rozmycia pasm (band broadening) wynikającego z obecności reaktora.
- Wady:
- Wymagana wysoka stabilność pochodnej.
- Produkty uboczne reakcji mogą interferować z innymi analitymi na kolumnie.
Derywatyzacja pokolumnowa (Post-column)
Reakcja zachodzi w sposób ciągły w reaktorze umieszczonym pomiędzy kolumną a detektorem. Eluent opuszczający kolumnę jest mieszany ze strumieniem odczynnika.
- Zalety:
- Stabilność pochodnej nie jest krytyczna (musi przetrwać jedynie sekundy w drodze do detektora).
- Analit jest rozdzielany w swojej natywnej postaci, co ułatwia optymalizację separacji.
- Brak wpływu nadmiaru odczynnika na proces rozdziału
- Wady:
- Konieczność stosowania dodatkowych pomp i precyzyjnych reaktorów (koszt aparatury).
- Ryzyko rozmycia stref chromatograficznych w reaktorze.
- Ograniczenie do szybkich reakcji (kinetyka musi być rzędu sekund/minut).
Mechanizmy chemiczne derywatyzacji
Zrozumienie chemii organicznej stojącej za derywatyzacją jest niezbędne do poprawnej optymalizacji metody. Wybór odczynnika zależy od obecności konkretnych grup funkcyjnych w analizowanym związku.
Nukleofilowa substytucja i addycja
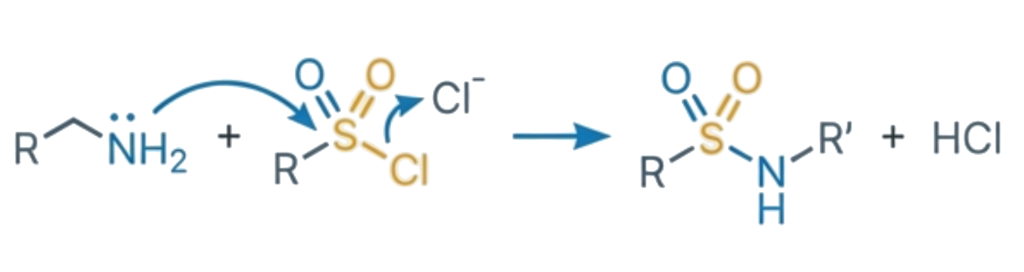
Najczęstszą grupą docelową są aminy (pierwszo- i drugorzędowe). Wykorzystuje się tu ich charakter nukleofilowy.
- Przykład: Reakcja amin z chlorkami sulfonylu (np. Dansyl-Cl) lub chloromrówczanami (np. FMOC-Cl). Reakcja ta przebiega sprawnie w środowisku lekko zasadowym.
Kondensacja
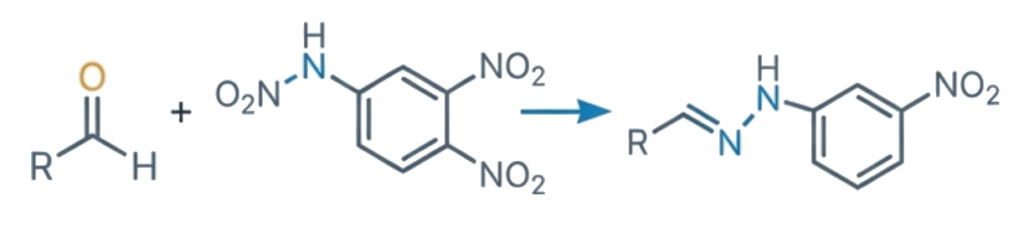
Stosowana głównie dla grup karbonylowych (aldehydy, ketony) oraz amin.
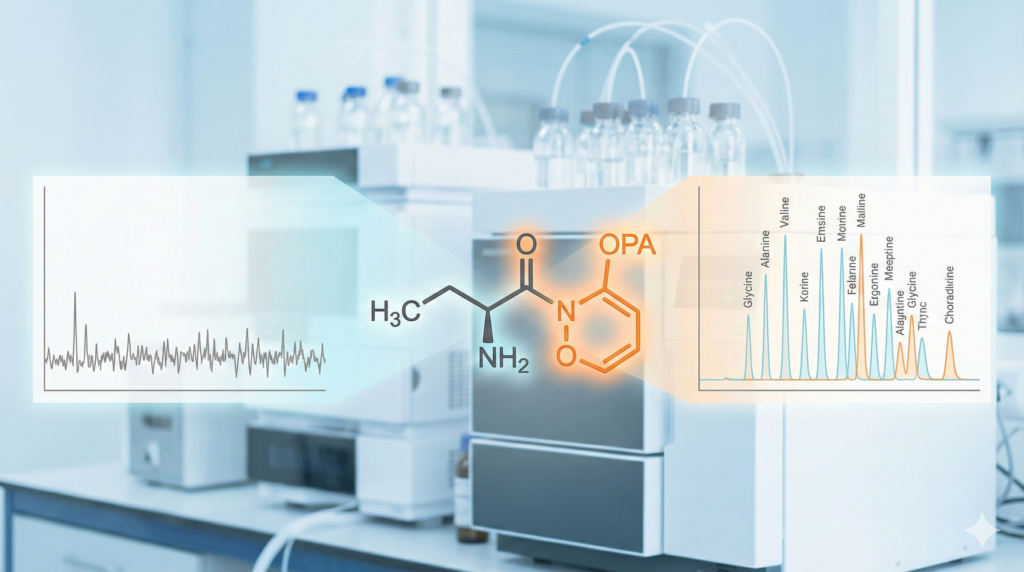
- Przykład: Reakcja aldehydów z 2,4-dinitrofenylohydrazyną (DNPH) prowadząca do powstania hydrazonów absorbujących w UV. Innym przykładem jest reakcja OPA (o-ftaloaldehydu) z aminami w obecności tiolu (np. 2-merkaptoetanolu), tworząca fluorescencyjne pochodne izoindolu.
Reakcje z grupami tiolowymi (-SH)
Tiole są niezwykle reaktywne i podatne na utlenianie do disiarczków. Derywatyzacja za pomocą odczynników takich jak monobromobiman (mBBr) pozwala na ich stabilizację i ultra-czułą detekcję fluorescencyjną.
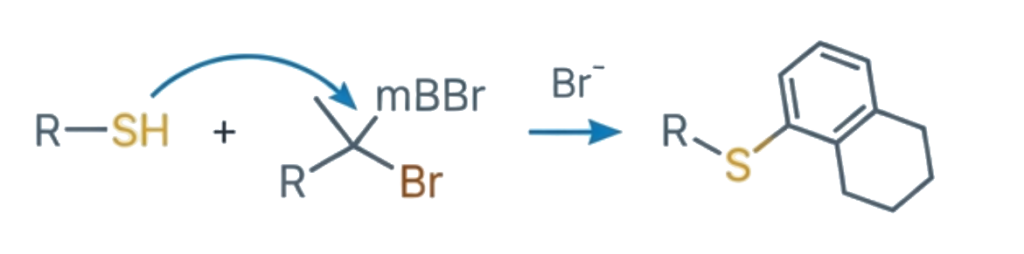
Przegląd kluczowych odczynników i zastosowań praktycznych
W tabeli poniżej przedstawiam zestawienie odczynników, które na stałe wpisały się w kanon analityki HPLC.
| Odczynnik | Grupa docelowa | Detekcja | Zastosowanie | Charakterystyka pochodnej |
| OPA (o-ftaloaldehyd) | Aminy 1° | FLD | Aminokwasy, histamina | Niestabilna, wymaga natychmiastowego nastrzyku |
| FMOC-Cl | Aminy 1° i 2° | FLD/UV | Glikofosat, aminokwasy | Bardzo stabilna, nadmiar wymaga usunięcia |
| Dansyl-Cl | Aminy, Fenole | FLD | Pestycydy, aminy biogenne | Szerokie spektrum, długa faza wzbudzenia |
| Ninhydryna | Aminy (α-aminokwasy) | UV-Vis (570 nm) | Analiza kliniczna aminokwasów | Klasyczna metoda pokolumnowa |
| Dabsyl-Cl | Aminy | UV-Vis | Oznaczanie białek | Wysoki współczynnik absorpcji w świetle widzialnym |
| DNPH | Aldehydy/Ketony | UV | Analiza formaldehydu w powietrzu | Stabilne hydrazony, doskonała selektywność |
Studium przypadku: Analiza aminokwasów metodą OPA vs FMOC
Analiza aminokwasów to klasyczny przykład, gdzie derywatyzacja jest niezbędna.
- Metoda OPA: Jest niezwykle szybka (reakcja w 1-2 minuty), co pozwala na automatyzację in-needle (w igle autosamplera). Jednak OPA nie reaguje z aminami drugorzędowymi (np. proliną).
- Metoda FMOC: Reaguje z proliną, co czyni ją bardziej uniwersalną. Jednakże produkt uboczny – alkohol FMOC – jest silnie fluorescencyjny i może maskować piki analitów, co wymusza dodatkowy etap płukania lub ekstrakcji.
6. Porównanie techniczne – Tabela podsumowująca
Dla inżyniera procesu i analityka, wybór między techniką przed- a pokolumnową jest decyzją strategiczną.
| Parametr | Derywatyzacja Przedkolumnowa | Derywatyzacja Pokolumnowa |
| Wpływ na retencję | Zmienia czas retencji (zwykle zwiększa) | Brak wpływu na separację na kolumnie |
| Wymagania aparatury | Standardowy zestaw HPLC/UHPLC | Dodatkowe pompy, reaktor, termostat |
| Czas reakcji | Może być długi (minuty/godziny) | Musi być bardzo krótki (sekundy) |
| Stabilność produktu | Musi być wysoka (min. godziny) | Może być bardzo niska |
| Czystość próbki | Możliwe interferencje odczynnika | Odczynnik nie wpływa na selektywność kolumny |
| Łatwość obsługi | Wysoka (często automatyczna) | Średnia (wymaga walidacji hydrodynamiki) |
Czy derywatyzacja ma sens w dobie MS?
Jako, że przez wiele lat pracowałem z detektorami mas, patrzyłem na derywatyzację jako relikt przeszłości. Coś, co zostanie prędzej czy później odstawione jako niepotrzebny wysiłek. Nic bardziej mylnego.
Po pierwsze detekcja to nie jedyny powód derywatyzacji. Może przecież wspomagać sam rozdział chromatograficzny lub stabilizować analit. W takim przypadku sposób detekcji nie wpłynie na konieczność przeprowadzania reakcji.
Po drugie, derywatyzacja może zwiększyć wydajność jonizacji a tym samym czułość instrumentu. Cząstki polarne takie jak aminokwasy czy cukry po przyłączeniu hydrofobowego „tagu”, lepiej przechodzą w fazę gazową i się jonizują. Dobrym przykładem jest analiza glikanów z wykorzystaniem Rapi-Fluor-MS™. Derywatyzację przeprowadza się przed naniesieniem na kolumnę. Przyłączona grupa umożliwia detekcję glikanów w detektorze FLD i umożliwia ich silną jonizację w ESI. Daje to możliwość określenia dokładnej struktury glikanów.
Po trzecie, derywatyzacja w UV/FLD jest znacznie bardziej odporna na efekty matrycowe (tłumienie sygnału) niż LC-MS, co jest kluczowe w analizie próbek środowiskowych i klinicznych.
Podsumowanie
Derywatyzacja to nie tylko „farbowanie” cząsteczek. To precyzyjne projektowanie właściwości chemicznych analitu pod konkretny problem analityczny. Wykonując ją należy pamiętać o kilku rzeczach:
- Kontroli pH: Większość reakcji derywatyzacji jest silnie zależna od pH środowiska (szczególnie ataki nukleofilowe amin).
- Czystości odczynników: Zanieczyszczenia w odczynniku derywatyzującym generują tzw. piki „duchy”.
- Kinetyce: Zawsze sprawdzaj, czy czas reakcji w autosamplerze jest powtarzalny i wystarczająco długi.
Derywatyzacja pozostaje fundamentem nowoczesnej analityki, łącząc klasyczną chemię organiczną z zaawansowaną technologią rozdziałów.
Bibliografia i źródła uzupełniające
- Meyer V. R., Practical High-Performance Liquid Chromatography, 5th Edition, Wiley, 2010.
- Snyder L. R., Kirkland J. J., Dolan J. W., Introduction to Modern Liquid Chromatography, 3rd Edition, Wiley, 2009.
- Mou D. Determination of Amino Acids By Precolumn Derivatization with o – phtaldialdehyde (OPA) and Reversed-phase High Performance Liquid Chromatography. Se Pu. 1997
- Harris E.L. Amino Acid Analysis by Precolumn Derivatization. Methods Mol Biol. 1988
- Raynie D. E. Analyte Derivatization as an Important Tool for Sample Preparation, LCGC North America, Vol 36, 2018
