HPLC, czyli wysokosprawna chromatografia cieczowa jest techniką analityczną, bez której nie istnieje współczesny przemysł farmaceutyczny i chemiczny. Dziś tysiące, przeróżnych aparatów HPLC stoi w laboratoriach badawczych i kontroli jakości zakładów przemysłowych i badawczych na całym świecie. Ten artykuł jest pierwszym z serii poświęconej HPLC ma za zadanie wprowadzić do tego tematu.

Co to jest HPLC?
Chromatografia sama w sobie jest metodą rozdziału mieszanin na poszczególne składniki dzięki ich różnemu powinowactwu do dwóch faz: fazy ruchomej (eluentu) oraz fazy stacjonarnej (wypełnienia kolumny). Więcej na ten temat znajdziesz w tym artykule.
Różnica między chromatografią klasyczną a HPLC
W klasycznej chromatografii cieczowej (kolumnowej), faza ruchoma przemieszcza się przez kolumnę pod wpływem niewielkich sił. Może to być siła grawitacji lub niewielki przepływ uzyskany dzięki pompie. Jest to proces powolny i charakteryzuje się niską rozdzielczością.
W HPLC sytuacja ulega drastycznej zmianie. Kluczem do sukcesu jest zastosowanie bardzo drobnego ziarna wypełnienia (zazwyczaj od 1,8 do 5 μm). Im mniejsze ziarno, tym większa powierzchnia wymiany i lepsza separacja, ale jednocześnie tym większy opór stawiany przepływającej cieczy. Aby go pokonać, konieczne jest zastosowanie wysokiego ciśnienia (sięgającego 400 barów w klasycznym HPLC i ponad 1000 barów w układach UHPLC). Dzięki zastosowaniu drobnego ziarna uzyskuje się większą zdolność rozdzielczą, skraca się czas analizy. Ogólnie kolumny do HPLC są mniejsze niż kolumny do niskociśnieniowej chromatografii. Dzięki temu możliwe jest zmniejszenie ilości próbki koniecznej do analizy.
Jak zbudowane jest HPLC?
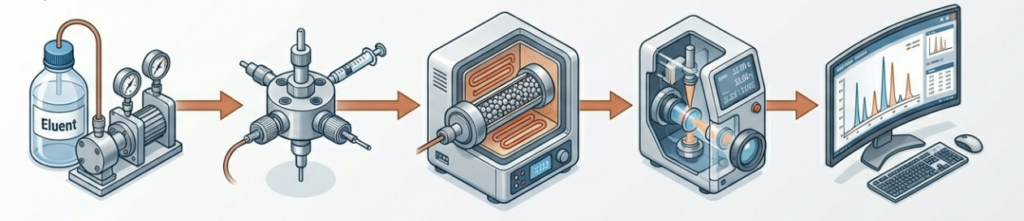
Aparat do HPLC, nazywany potocznie chromatografem, to zaawansowany system modułowy. Każdy z elementów pełni krytyczną rolę w procesie analitycznym.
Pompy (Układ dostarczania rozpuszczalnika)
Pompa to podstawa układu. Musi dostarczać fazę ruchomą ze stałym natężeniem przepływu (np. 1 ml/min) pod wysokim ciśnieniem. Ważne by przepływ fazy ruchomej był stabilny, bez pulsacji.
Pompa może pracować w dwóch różnych trybach: izokratycznym i gradientowym. Takie też wyróżnia się rodzaje elucji:
- Izokratyczną: Skład fazy ruchomej jest stały podczas całej analizy.
- Gradientową: Skład fazy zmienia się w czasie (np. rośnie stężenie rozpuszczalnika organicznego), co pozwala na szybszy rozdział skomplikowanych mieszanin.
Dozownik (Iniektor)
Miejsce wprowadzenia próbki do układu. W prostych HPLC rolę iniektora pełni port strzykawki wraz z pętlą iniekcyjną. Zadaniem pętli jest precyzyjna kontrola nad objętością próbki wprowadzonej do układu.
Współcześnie stosuje się autosamplery, które automatycznie pobierają precyzyjną objętość i wprowadzają ją do strumienia eluentu pod wysokim ciśnieniem za pomocą specjalnego zaworu (typu Rheodyne). Zaletą autosamplerów jest wygoda (operator nie musi ręcznie wprowadzać próbki przed każdą analizą) oraz wydajność (pozwalają zautomatyzować pracę i ustawić kolejkę nawet wielu tysięcy próbek)
Kolumna chromatograficzna
Najważniejszy element, w którym dochodzi do właściwego rozdziału. Często umieszczana w tzw. Piecu (czyli termostabilizowanym pojemniku na kolumny), aby utrzymać stałą temperaturę, co wpływa na powtarzalność czasów retencji. Piec umożliwia również podgrzanie lub schłodzenie kolumny. Temperatura może znacząco wpływać na zdolność rozdzielczą kolumny. Chłodzenie umożliwia analizę związków termolabilnych.
Detektor
Urządzenie monitorujące skład wycieku z kolumny. Wśród najczęściej stosowanych detektorów są:
- UV-Vis / DAD (Diode Array Detector): Mierzy absorbancję światła przez związki chemiczne.
- Fluorescencyjny: Bardzo czuły, dla związków zdolnych do fluorescencji.
- Masowy (MS): Pozwala na identyfikację struktury cząsteczek.
Układ rejestrujący (System danych)
Oprogramowanie zbierające sygnały z detektora i przetwarzające je na chromatogram – wykres zależności sygnału od czasu.
Budowa i rola kolumny HPLC
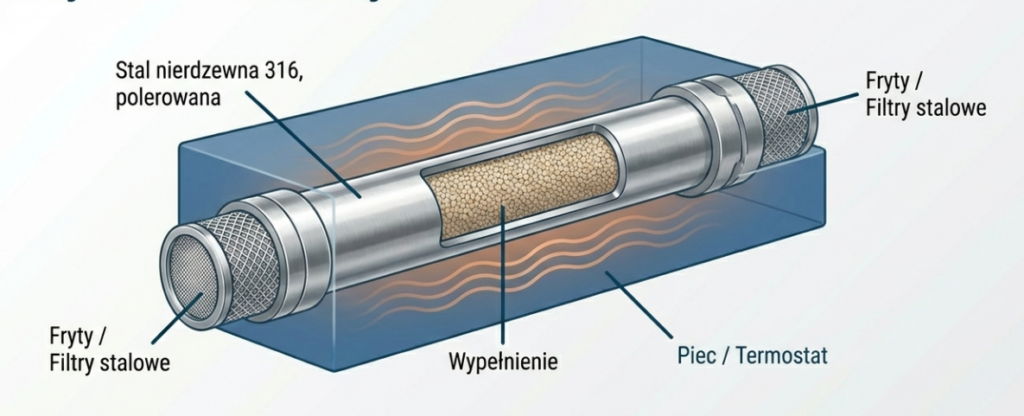
Kolumna do HPLC to precyzyjny przyrząd inżynieryjny, który musi wytrzymać ogromne naprężenia mechaniczne i chemiczne.
Stalowa obudowa
Zewnętrzna część kolumny wykonana jest z wysokogatunkowej stali nierdzewnej (zazwyczaj typu 316), polerowanej wewnątrz, aby zminimalizować tarcie i turbulencje przepływu.
Wypełnienie (Faza stacjonarna)
Najczęściej jest to żel krzemionkowy (silica gel). Żel ma postać ziaren o porowatej strukturze. Powierzchnia krzemionki jest modyfikowana chemicznie poprzez przyłączanie różnych grup funkcyjnych, co decyduje o charakterze oddziaływań z analitami. Dostępne są również kolumny z jednolitym wypełnieniem
Fryty (Filtry porowate)
Na obu końcach kolumny znajdują się stalowe fryty. Ich zadaniem jest:
- Utrzymanie wypełnienia wewnątrz kolumny.
- Wstępne filtrowanie próbki i fazy ruchomej, aby zapobiec zapchaniu drobnego ziarna.
Rodzaje kolumn i mechanizmy rozdziału
Wybór kolumny zależy od właściwości fizykochemicznych badanych substancji.
Faza Odwrócona (Reverse Phase – RP)
To najpowszechniejsza technika (ok. 80% wszystkich analiz).
- Faza stacjonarna: Niepolarna (np. łańcuchy węglowe C18, C8).
- Faza ruchoma: Polarna (woda, metanol, acetonitryl).
- Zasada: Związki bardziej polarne eluują (wypływają) jako pierwsze, a te bardziej „tłuste” (hydrofobowe) zatrzymują się dłużej.
Faza Normalna (Normal Phase – NP)
Historycznie pierwsza, dziś stosowana rzadziej (np. do rozdziału izomerów).
- Faza stacjonarna: Polarna (czysta krzemionka).
- Faza ruchoma: Niepolarna (heksan, heptan).
- Zasada: Związki niepolarne wypływają szybko, polarne są silnie zatrzymywane.
Chromatografia Jonowymienna (IEX)
Służy do rozdziału jonów i cząsteczek posiadających ładunek (np. białka, aminokwasy). Wykorzystuje przyciąganie elektrostatyczne między analitem a naładowanymi grupami na powierzchni wypełnienia.
Chromatografia Wykluczania (SEC / GPC)
Rozdział następuje ze względu na wielkość cząsteczek. Większe molekuły, które nie mieszczą się w porach wypełnienia, omijają je i wypływają najszybciej. Małe cząsteczki „wchodzą” do labiryntu porów, co wydłuża ich drogę.

Rodzaje HPLC i jego zastosowanie
Czytając ten artykuł HPLC ukazuje się jako doskonałe narzędzie analityczne. Faktycznie, największe zastosowanie ma właśnie w laboratoriach analitycznych. Oto dziedziny w jakich znalazło zastosowanie
Zastosowanie HPLC w analityce
- Farmacja: Kontrola czystości leków, badanie trwałości substancji czynnych, monitorowanie stężenia leków we krwi (TDM).
- Analiza żywności: Wykrywanie aflatoksyn, oznaczanie zawartości witamin, konserwantów czy kofeiny w napojach.
- Diagnostyka medyczna: Oznaczanie poziomu hormonów, markerów nowotworowych oraz badania przesiewowe noworodków.
- Kryminalistyka i Toksykologia: Wykrywanie narkotyków, dopingu oraz trucizn w materiale biologicznym.
Jak widać zastosowań analitycznych jest mnóstwo, jednak to nie wszystko. HPLC, jak każda chromatografia jest techniką separacyjną. Umożliwia rozdzielenie różnych substancji. Tą zdolność można wykorzystać również w celu oczyszczania substancji.
Zastosowanie HPLC w preparatyce
- HPLC preparatywne: Dzięki zastosowaniu kolumn o większej średnicy i kolektora frakcji możliwe jest rodzielanie substancji chemicznych w celu ich oczyszczenia. Skala preparatywna umożliwia oczyszczanie sustancji w ilości od miligramów do gramów. Ma zastosowanie w laboratoriach badawczych i rozwojowych, w szczególności w przemyśle chemicznym i bitoechnologicznym
- HPLC przemysłowe: W tym przypadku kolumny chromatografii są jeszcze większe a pompy przystosowane do większych przepływów. Układy przemysłowe wykorzystywane są do skutecznego oczyszczania na dużą skalę np. w biotechnologicznych zakładach przemysłowych. Umożliwiają oczyszczanie dziesiątek a nawet setek gramów substancji (np. białek).
Podsumowanie
Mam nadzieję, że ten artykuł przybliżył Ci trochę podstawę działania HPLC. Więcej o teorii rozdziału, rodzajach kolumn i typach rozdziałów znajdziesz w kolejnych artykułach z tego cyklu.
Literatura:
- Kocjan R. (red.), Chemia analityczna. Analiza instrumentalna, Wydawnictwo Lekarskie PZWL.
- Namieśnik J., Jamrógiewicz Z., Pilarczyk M., Torres L., Przygotowanie próbek środowiskowych do analizy, Wydawnictwa Naukowo-Techniczne.
- Walenty Szczepaniak, Metody Instrumentalne w analizie chemicznej, Wydawnictwo Naukowe PWN
Grafika
Cyberwork 95, CC BY-SA 4.0 <https://creativecommons.org/licenses/by-sa/4.0>, via Wikimedia Commons
